���P(gu��n)��(x��)�}
0 10192 10200 10206 10210 10216 10218 10222 10228 10230 10236 10242 10246 10248 10252 10258 10260 10266 10270 10272 10276 10278 10282 10284 10286 10287 10288 10290 10291 10292 10294 10296 10300 10302 10306 10308 10312 10318 10320 10326 10330 10332 10336 10342 10348 10350 10356 10360 10362 10368 10372 10378 10386 203614
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ����x�}
X�cY��Ԫ�ص��(y��ng)�x�Ӿ�����ͬ����ӌӽY(ji��)��(g��u)��X Ԫ�ص��(y��ng)�x�Ӱ돽����YԪ�ص��(y��ng)�x�Ӱ돽���Y�cZ��Ԫ�صĺ�����ӌӔ�(sh��)��ͬ��ZԪ�صĵ�һ��x�ܴ���YԪ�صĵ�һ��x����������tX�������Y����Z��ԭ����(sh��)
A��X>Y>Z
B��Y>X>Z
C��Z>X>Y
D��Z>Y>X
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ�����}
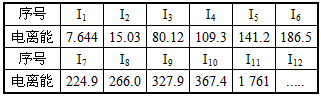
��֪��x����ָ1 mol��B(t��i)ԭ�ӣ����(y��ng)�x�ӣ�ʧȥ l mol����γ���l mol��B(t��i)�(y��ng)�x�ӣ�����߃r(ji��)�(y��ng)�x�ӣ�����Ҫ���յ�����������F(xi��n)�к�늺ɔ�(sh��)С��20��Ԫ��A������x�ܔ�(sh��)��(j��)���£�(I1��ʾ��B(t��i)ԭ��ʧȥ��һ��(g��)��ӵ���x���������In��ʾ�x��ʧȥ��n��(g��)��ӵ���x���������λ��eV)
(1)�������x��Խ�h(yu��n)�������Խ�ߣ���x��Խ___________���� ����С���������(y��ng)�x��늺ɔ�(sh��)Խ�����������ʧȥ��ӕr(sh��)��������x��Խ___________�����С������
(2)����11��(g��)��ӷ�________��(g��)��ӌ��������
(3)ԓԪ�ص���Ҫ���σr(ji��)��_(k��i)________���
(4)ԓԪ��ԭ�ڵ�����Ų�ʽ��_(k��i)____________
(5)��(xi��)��ԓԪ����߃r(ji��)�����(du��)��(y��ng)��ˮ�����cϡ�}�ᷴ��(y��ng)���x�ӷ���ʽ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ģ�M�}
�}�ͣ�����}
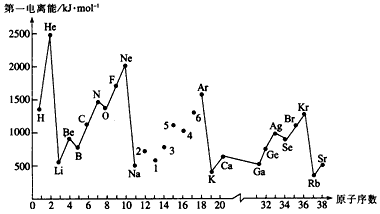
��һ��x��I1��ָ��B(t��i)ԭ��X(ju��)(g)̎�ڻ��B(t��i)�r(sh��)����ʧȥһ��(g��)��ӳɞ��B(t��i)�(y��ng)�x��X(ju��)+(g)��������������D�Dz���Ԫ��ԭ�ӵĵ�һ��x��I1�Sԭ����(sh��)׃���������D������12̖(h��o)��17̖(h��o)Ԫ�ص����P(gu��n)��(sh��)��(j��)ȱʧ������Ո(q��ng)�ش�����(w��n)�}��
(1)�J(r��n)������ψD��ͬ����Ԫ�ص�һ��x�ܵ�׃��Ҏ(gu��)�ɣ��Ɣ�Na-ArԪ�������Al�ĵ�һ��x�ܵĴ�С������������������� ____< Al<____����Ԫ�ط�̖(h��o)���������Al��ԭ�����������Ų�ʽ��_(k��i)________________����
(2)���ψD������֪�������ͬһ����Ԫ��ԭ�ӵĵ�һ��x��I1׃��Ҏ(gu��)����_________________________�����
(3)�ψD�е�һ��x����С��Ԫ�������ڱ��е�λ����__________________��
(4)����(j��)��(du��)�Ǿ�Ҏ(gu��)�t����Be������AlԪ�����������ˮ��������|(zh��)���ƣ�����������___________�ԣ�����Be(OH)2�@ʾ�@�N���|(zh��)���x�ӷ���ʽ�ǣ�_________________________________�������____________________________����
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ������(xi��ng)�x���}
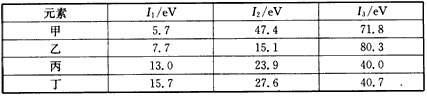
��B(t��i)����ԭ��ʧȥһ��(g��)����D(zhu��n)�����B(t��i)���x������Ҫ���������������һ��x��(I1)������B(t��i)���x���^�m(x��)ʧȥ�����������������ηQ��ڶ���x��(I2)�����������x��(I3)�����±��ǵ������ڲ���Ԫ�ص���x��[��λ�� eV(��ӷ���)]��(sh��)��(j��)�����
�����f(shu��)�����_����
A���Ľ����Ա��ҏ�(qi��ng)
B���ҵĻ��σr(ji��)��+1�r(ji��)
C����һ����ǽ���Ԫ��
D����һ���ǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ�����}
��x����ָ1mol��B(t��i)ԭ�ӣ����(y��ng)�x�ӣ�ʧȥ1mol����γ�1mol��B(t��i)�(y��ng)�x�ӣ�����߃r(ji��)�(y��ng)�x�ӣ��������յ��������F(xi��n)�к�늺ɔ�(sh��)С��20��Ԫ��A�������x�ܔ�(sh��)��(j��)���£���I1��ʾԭ��ʧȥ��1��(g��)��ӵ���x�ܣ�
In��ʾԭ��ʧȥ��n��(g��)��ӵ���x��������λ��eV��
(1)�������x��Խ�h(yu��n)�����������Խ��������x��Խ____�����С�����������(y��ng)�x��늺ɔ�(sh��)Խ�����������ʧȥ��ӕr(sh��)�����x��Խ____�����������С����
(2)����11��(g��)��ӷׂَ�(g��)��ӌӣ�____________
(3)ȥ��11��(g��)��Ӻ��������ԓԪ��߀��_______��(g��)�������
(4)ԓԪ����߃r(ji��)�����(du��)��(y��ng)ˮ����Ļ��W(xu��)ʽ��________���
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ����(zhu��n)�(xi��ng)�}
�}�ͣ����x�}
ijԪ�ص���x��(��ӷ���)���±�����Ԫ��λ��Ԫ�����ڱ����唵(sh��)��
A.��A
B.��A
C.��A
D.��A
E. ��A
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ�����}
��ͬԪ�صĚ�B(t��i)ԭ��ʧȥ�����һ��(g��)�������Ҫ���������O(sh��)���E����D��ʾ����ԇ����(j��)Ԫ�������ڱ��е�λ�������������D��������׃�����c(di��n)����������ش����І�(w��n)�}��
(1)ͬ�����(n��i)��ͬԪ�ص�Eֵ׃�������c(di��n)��____________________������������Eֵ���@�N׃�����c(di��n)�w�F(xi��n)��Ԫ�����|(zh��)��____________׃��Ҏ(gu��)������
(2)ͬ���ڃ�(n��i)�����Sԭ����(sh��)��������Eֵ�����������(g��)�eԪ�ص�Eֵ���F(xi��n)�����F(xi��n)��������ԇ�A(y��)�y(c��)�����P(gu��n)ϵ�����_����
____���(xi��)��̖(h��o)��
��E���飩>E������ ��E���飩<E������ ��E���壩>E������ ��E���壩<E������
(3)��Ӌ(j��)1mol��B(t��i)Caԭ��ʧȥ�����һ��(g��)�����������Eֵ�ķ���____<E<____��
(4)10̖(h��o)Ԫ��Eֵ�^���ԭ��__________�������
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ�����}
��һ��x��I1��ָ��B(t��i)ԭ��X(ju��)(g)ʧȥһ��(g��)��ӳɞ��B(t��i)�(y��ng)�x��X(ju��)+(g)�������������D�Dz���Ԫ��ԭ�ӵĵ�һ��x��I1�Sԭ����(sh��)׃���������D��
Ո(q��ng)�ش�����(w��n)�}��
(1)�J(r��n)������ψD��ͬ����Ԫ�ص�һ��x�ܵ�׃��Ҏ(gu��)��������Na��Ar���NԪ���ö̾��B������(l��i)���������(g��u)�������ĈD��
(2)���ψD������֪�����ͬһ����Ԫ��ԭ�ӵĵ�һ��x��I1׃��Ҏ(gu��)����________����
(3)�ψD��5̖(h��o)Ԫ����Ԫ�����ڱ��е�λ����________���___________������
(4)�ψD��4��5������6���NԪ�صĚ�B(t��i)�仯��ķ��c(di��n)����ͬ������һ���ڵ�Ԫ�ؚ�B(t��i)�仯��ͺܶ࣬ԭ����
________________________���
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ������(xi��ng)�x���}
�����f(shu��)�����_����
A��Ԫ�صĵ�һ��x��Խ��ԓԪ��ԭ��Խ�yʧȥ��һ��(g��)���
B��ͬһ����������S��ԭ����(sh��)����������Ԫ�صĵ�һ��x��һ������
C��ͬһ�����������S����ӌӔ�(sh��)�����ӣ�Ԫ�صĵ�һ��x������
D��Ԫ�صĵ�һ��x�ܲ����Á�(l��i)����Ԫ�طǽ����Եď�(qi��ng)��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ������(xi��ng)�x���}
���и��MԪ�������ԭ�Ӱ돽���ΜpС����Ԫ�ص�һ��x����u���ߵ�������е���
A.K���Na��Li
B.Al�����Mg�������Na
C.N����O�������C
D.Cl������S�����P
�鿴�𰸺ͽ���>>