
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �ڢۢܢ� | B�� | �٢ۢ� | C�� | �٢ڢۢ� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
| A�� | ��Һ��c��NH4+���x�ӝ�� | B�� | ��ˮ����x�̶� | ||
| C�� | ˮ���x�ӷe����(sh��) | D�� | c��H+��/c��NH3•H2O�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
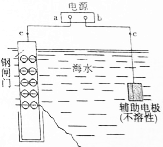 �������ճ�������r(n��ng)�I(y��)���a(ch��n)�ЏV��ʹ�õIJ��ϣ�ǡ��?sh��)Ľ��ٷ������������L���ٲ���ʹ�É�����ǰ�ᣮ
�������ճ�������r(n��ng)�I(y��)���a(ch��n)�ЏV��ʹ�õIJ��ϣ�ǡ��?sh��)Ľ��ٷ������������L���ٲ���ʹ�É�����ǰ�ᣮ�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
| A�� | ��������HI��HClO | B�� | ��������HCl��HIO | ||
| C�� | �����ÓQ���� | D�� | ���ڏͷֽⷴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | 0.025mol | B�� | 0.05mol | C�� | 0.075mol | D�� | 0.10mol |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
| ��A | ��A | ��A | ��A | VA | ��A | ��A | 0 | |
| ��2���� | �� | �� | ||||||
| ��3���� | �� | �� | �� | �� | �� | |||
| ��4���� | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �c��ˮ������2Na+2H2O�T2Na++2OH-+H2�� | |
| B�� | �F�۸�ϡ���ᷴ����2Fe+6H+�T2Fe3++3H2�� | |
| C�� | �������^��Һ��ϡ���ᷴ����Ba2++SO42-�TBaSO4�� | |
| D�� | ̼���}���}�ᷴ����CO32-+2H+�TH2O+CO2�� |
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com