
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | Na2O2 | B�� | H2O | C�� | MgCl2 | D�� | N2 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | SO42�� | B�� | Mg2+ | C�� | CH3COO- | D�� | OH�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | Clԭ�ӵĽY(ji��)��(g��u)ʾ��D��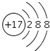 | |
| B�� | ����ĽY(ji��)��(g��u)ʽ��C2H4O2 | |
| C�� | �Ȼ�����ӵ����ʽ�� | |
| D�� | �����c����x����ʽ��Na2SO4�T2Na++SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | H2 | B�� | NO2 | C�� | NO | D�� | SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | ϡ��������~Ƭ�ϣ�Cu+2H+�TCu2++H2�� | |
| B�� | �����c��Һ�c�Ȼ��^��Һ��ϣ�Ba2++SO42-�TBaSO4�� | |
| C�� | �}�����ʯ��ʯ�ϣ�CaCO3+2H+�TH2CO3+Ca2+ | |
| D�� | �����~�c�����ϣ�Cu2++SO42-�TCuSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | H2��O2����(y��ng)������H2O | B�� | Zn��Ͷ��ϡ������ | ||
| C�� | KMnO4�ӟ���O2 | D�� | C��O2����(y��ng)����CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | �ڢۢ� | B�� | �ڢ٢� | C�� | �ڢۢ� | D�� | �ڢ٢� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | CO2 | B�� | NaCl | C�� | BaSO4 | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com