
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| ������ | ��ʼ�ض�t1���棩 | ĩ�ض�t2���棩 | �к͟ᣨkJ?mol-1�� |
| HCl+NaOH | 13.0 | 16.4 | ��H1 |
| HCl+NH3?H2O | 13.0 | 16.0 | ��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
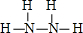
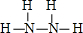
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
 ��D��NO2��g����CO��g����������CO2��g����NO��g���^��������׃��ʾ��D��
��D��NO2��g����CO��g����������CO2��g����NO��g���^��������׃��ʾ��D���鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com