
о}ДҝБРұн(°ьАЁҙр°ёәНҪвОц)
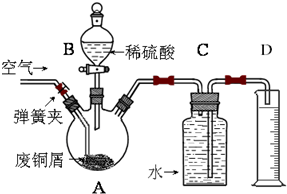
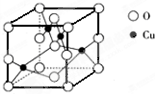 і¬јҡг~·ЫЦчТӘ‘Ә(yЁ©ng)УГУЪҢ§лҠІДБПЎўҙЯ»Ҝ„©өИоI(lЁ«ng)УтЦРЈ®і¬јҡг~·ЫөДДіЦЖӮд·Ҫ·ЁИзПВЈә
і¬јҡг~·ЫЦчТӘ‘Ә(yЁ©ng)УГУЪҢ§лҠІДБПЎўҙЯ»Ҝ„©өИоI(lЁ«ng)УтЦРЈ®і¬јҡг~·ЫөДДіЦЖӮд·Ҫ·ЁИзПВЈә
2- 3 |
| ||
| ||
| ||
| ||

| ||
| ||
| 11200n |
| V |
| 11200n |
| V |
°Щ¶ИЦВРЕ - ҫҡБ•ғФБРұн - ФҮо}БРұн
әюұұКЎ»ҘВ“(liЁўn)ҫW(wЁЈng)Я`·ЁәНІ»БјРЕПўЕeҲуЖҪЕ_ | ҫW(wЁЈng)ЙПУРәҰРЕПўЕeҲуҢЈ…^(qЁұ) | лҠРЕФpт_ЕeҲуҢЈ…^(qЁұ) | ЙжҡvК·М“ҹoЦчБxУРәҰРЕПўЕeҲуҢЈ…^(qЁұ) | ЙжЖуЗЦҷа(quЁўn)ЕeҲуҢЈ…^(qЁұ)
Я`·ЁәНІ»БјРЕПўЕeҲулҠФ’Јә027-86699610 ЕeҲуа]ПдЈә58377363@163.com