
科目: 來源:專項題 題型:單選題
查看答案和解析>>
科目: 來源:專項題 題型:單選題
查看答案和解析>>
科目: 來源:專項題 題型:填空題


查看答案和解析>>
科目: 來源:山東省期中題 題型:單選題
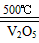 2SO3 △H=-196.6kJ·mol-1
2SO3 △H=-196.6kJ·mol-1查看答案和解析>>
科目: 來源:同步題 題型:不定項選擇題
 ΔH=-226 kJ/mol
ΔH=-226 kJ/mol 
查看答案和解析>>
科目: 來源:同步題 題型:單選題
[ ]
查看答案和解析>>
科目: 來源:同步題 題型:填空題
查看答案和解析>>
科目: 來源:0115 期中題 題型:填空題
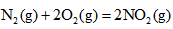 △H=+67.7kJ·mol-1
△H=+67.7kJ·mol-1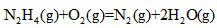 △H=-543kJ·mol-1
△H=-543kJ·mol-1 △H=-269kJ·mol-1
△H=-269kJ·mol-1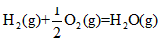 △H=-242kJ·mol-1
△H=-242kJ·mol-1 查看答案和解析>>
科目: 來源:北京期末題 題型:填空題

查看答案和解析>>
科目: 來源:北京期末題 題型:填空題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com