
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:

查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
 的化合物與CH2═CH2一樣,在一定條件下可聚合成高分子化合物.廣泛用作農(nóng)用薄膜的聚氯乙烯塑料屬于
的化合物與CH2═CH2一樣,在一定條件下可聚合成高分子化合物.廣泛用作農(nóng)用薄膜的聚氯乙烯塑料屬于 聚合而成的,其化學(xué)方程式是
聚合而成的,其化學(xué)方程式是查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:

查看答案和解析>>
科目: 來源: 題型:


| 壓強p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol?L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目: 來源: 題型:
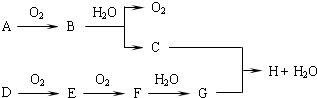
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com