

��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | �ڢۢߢ��� | B�� | �٢ڢۢݢ�� | C�� | �ڢݢޢߢ� | D�� | �ڢܢߢ�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
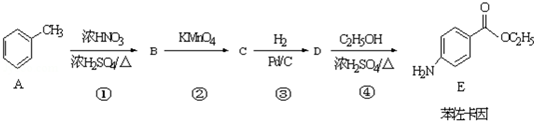
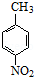 ��
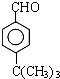
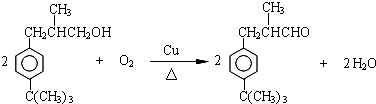
��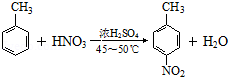 ������(y��ng)�ܵĻ��W(xu��)����ʽ��
������(y��ng)�ܵĻ��W(xu��)����ʽ��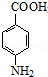 +CH3CH2OH
+CH3CH2OH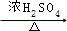
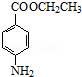 +H2O��
+H2O��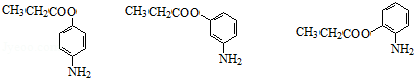 �����Ό�(xi��)һ�N��
�����Ό�(xi��)һ�N���鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | ����ƿ��ԭ���������sˮ | |
| B�� | ϴ������Ͳ���������Һδ�D(zhu��n)������ƿ�� | |
| C�� | ���ݕr(sh��)�^(gu��n)��Һ�温ҕ | |
| D�� | �Q(ch��ng)���õ����a�����P |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
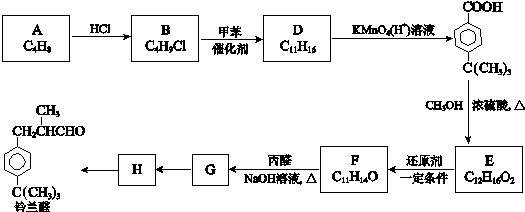
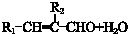
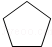
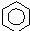 $\stackrel{����}{��}$
$\stackrel{����}{��}$ 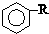 +HCl
+HCl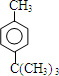 ��
�� ��
�� ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
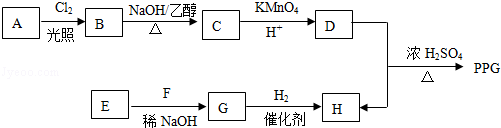
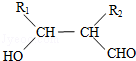
 ��
��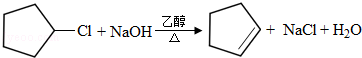 ��
��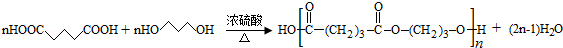 ��
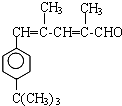
��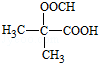 ����(xi��)��(g��u)��(ji��n)ʽ��
����(xi��)��(g��u)��(ji��n)ʽ���鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
| A�� | 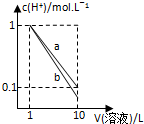 | B�� | 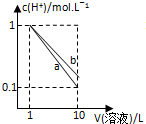 | C�� | 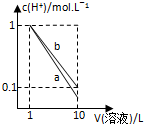 | D�� | 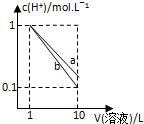 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
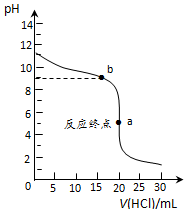
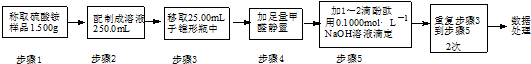
| �ζ��Δ�(sh��) | ���y(c��)��Һ�� �w�e/mL | ��(bi��o)��(zh��n)��Һ���w�e/mL | |
| �ζ�ǰ�̶� | �ζ���̶� | ||
| 1 | 25.00 | 0.00 | 20.01 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.30 | 20.30 |
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)��(zhu��n)�^(q��) | ����p�_�e��(b��o)��(zhu��n)�^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)��(zhu��n)�^(q��) | �����֙�(qu��n)�e��(b��o)��(zhu��n)�^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ(hu��)��027-86699610 �e��(b��o)�]�䣺58377363@163.com