���P(gu��n)��(x��)�}
0 10331 10339 10345 10349 10355 10357 10361 10367 10369 10375 10381 10385 10387 10391 10397 10399 10405 10409 10411 10415 10417 10421 10423 10425 10426 10427 10429 10430 10431 10433 10435 10439 10441 10445 10447 10451 10457 10459 10465 10469 10471 10475 10481 10487 10489 10495 10499 10501 10507 10511 10517 10525 203614
��Ŀ��
��(l��i)Դ������ʡģ�M�}
�}�ͣ��Ɣ��}
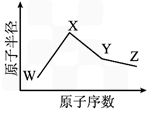
W������X��Y���Z��N�Ƕ�����Ԫ��������������ĺ�늺˔�(sh��)��������������
��1��W���|(zh��)�Ļ��W(xu��)ʽ��_(k��i)_________ ��ZԪ��ԭ�Ӻ�����__________��(g��)ԭ��܉����������������
��2��W��X�γɵĻ������еĹ��r(ji��)�I��ԭ��܉�����دB��ʽ����____________�I��
��3��Y�����Z��N���NԪ�ص�һ��x���ɴ�С�����?y��n)�_(k��i)_________����Ԫ�ط�̖(h��o)�����
��4��Z��X�γɵĻ����(g��u)�ɵľ��w����___________���w��
��5��Y���w�Ķѷe��ʽ���D��ʾ����������Yԭ�ӵ���λ��(sh��)��_(k��i)__________������
��6������늽�Y�cN���ڻ�����ķ������a(ch��n)Y���|(zh��)��ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ģ�M�}
�}�ͣ��Ɣ��}
��N������Ԫ��A������B��C�����D������E��ԭ����(sh��)�����������A��B����C���NԪ��ԭ�Ӻ�����ӌӔ�(sh��)֮ ����5������A��B��Ԫ��ԭ���������Ӕ�(sh��)֮�͵���CԪ��ԭ���������Ӕ�(sh��)�����BԪ��ԭ��������� ����Ӕ�(sh��)������ӌӔ�(sh��)��2������A��C�����γɻ�����CA3����B�cD��ԭ����(sh��)֮�Ȟ�3:4;EԪ ��ԭ���������Ӕ�(sh��)�ȴ������Ӕ�(sh��)��1���Ո(q��ng)�ش�
(1)��A�����B�ɷNԪ�ؽM�ɵķ����ж�N�����������һ�N���Ӻ�10��(g��)������������(xi��)�������ʽ___������
(2)���������A����B������C������D�ķNԪ�ؽM�������ȿ����c�}�ᷴ��(y��ng)�ֿ����cNaOH��Һ����(y��ng)������Ҽמ�o(w��) �C(j��)�}��������仯�W(xu��)ʽ��_(k��i)___�����
(3)��A��C������E���NԪ�ؽM�ɵĻ�����C2 A6 E2��һ�N��Ҫ�Ļ���ԭ�ϣ������x�ӻ�������������� ˮ����Һ�����������ˮ��ԭ���cNH4 Cl�����������(xi��)��ԓ�������һ��ˮ����x�ӷ���(y��ng)����ʽ___��
(4)�z�B(t��i)�����w���t(y��)�W(xu��)������Ҫ����;������{��(j��)Fe3O4�Ǵ����w�е���Ҫ���ӣ����Ƃ��^(gu��)�̿ɺ�(ji��n)�α�ʾ���£�
�ٌ�������CA3ͨ������|(zh��)������Fe3O4������Fe2(SO4)3�Ļ����Һ�У����ɃɷN�A�����(xi��)��ԓ����(y��ng)�^(gu��)���еĿ��x�ӷ���ʽ___����
����������(y��ng)���ɵăɷN�A�^�m(x��)���õõ�Fe3O4������ԓ����(y��ng)�Ļ��W(xu��)����ʽ��_(k��i)___��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ��Ɣ��}
��A�����B�����C��D����E��N������Ԫ������������ԭ����(sh��)����������֪��A��C������B��D�քeλ��ͬ�������������B�������D�|(zh��)�Ӕ�(sh��)֮����A�������C�|(zh��)�Ӕ�(sh��)֮�͵�2���������E��ͬ����Ԫ����ԭ�Ӱ돽�������
(1)B�γɵ��pԭ�ӷ��������������r(ji��)�I�������________��������A2B��Bԭ�Ӳ���________�s����
(2)A2B��A2D�ķ��c(di��n)�^������________(��W(xu��)ʽ)������ԭ����____________��
(3)Eԭ�ӵ�����Ų�ʽ��_(k��i)_______��
(4)��(xi��)���քe��A����B��C����D�ķNԪ�ؽM�ɵă����|(zh��)�ĝ���Һ�l(f��)������(y��ng)���x�ӷ���ʽ��_________________.
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ģ�M�}
�}�ͣ����x�}
X����Y����Z���W��ԭ����(sh��)����������ķN������Ԫ�أ������������������������������������еăɷN�����NԪ�ؽM�ɵĻ���������������ZԪ���γɵĆ��|(zh��)�������֪���� + �� = �� + �������� + �� = �� + �������� 0.1 mol��L-1����Һ��pH��13��25�棩�������f(shu��)���_����
A��ԭ�Ӱ돽��W��Z��Y��X
B��YԪ�������ڱ��е�λ�Þ�������ڵڢ�A��
C��1 mol���c����������ȫ����(y��ng)���D(zhu��n)����1 mol���
D��1.0 L 0.1 mol��L-1����Һ����x�ӿ������|(zh��)����С��0.1 mol
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ģ�M�}
�}�ͣ����x�}
ԭ����(sh��)���������X�������Y�������Z������W�ķN������Ԫ�أ�X�������Wԭ�ӵ��������Ӕ�(sh��)�c����ӌӔ�(sh��)������X��Z���������Ӕ�(sh��)֮���cY�������W���������Ӕ�(sh��)֮����ȡ��Ļ��W(xu��)ʽ��YX 3���������һ�N�̼��Ԛ�ζ�Ě��w�������ҵĻ��W(xu��)ʽ��YZ3��������X������Y��Z�M�ɵ��}��������f(shu��)�����_����
A��ԭ�Ӱ돽��W��Y��Z�����x�Ӱ돽�� Z��Y��W(w��ng)
B��W���Ȼ���ˮ��Һ�еμ��^(gu��)��Z�c�c�γɵĻ����������������ɻ�����Na3WZ6
C���y(c��)�ñ���ˮ��Һ������������t��Һ�б��}�(y��ng)�x�ӝ�ȴ�������x�ӝ��
D�����c(di��n)�h(yu��n)���������������Ǽ����g���ښ��I����
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ģ�M�}
�}�ͣ��Ɣ��}
X�����Y��Z�����W�ķN������Ԫ������������X��Y����Z��ԭ����(sh��)֮�͞�16������X��Y���Z���NԪ�صij�Ҋ(ji��n)���|(zh��)�ڳ��س����¶��ǟo(w��)ɫ���w�����m��(d��ng)?sh��)ėl���¿��l(f��)�����D��ʾ��׃���� ��֪һ��(g��)B�����к��е�ZԪ�ص�ԭ�ӂ�(g��)��(sh��)��һ��(g��)C��������һ��(g��)�������W�Ć��|(zh��)�ڳ��س�������w���������WԪ�����γɻ�����N�����Ԫ�ء�Ո(q��ng)�ش����І�(w��n)�}��
��1��Ԫ��X�����ڱ��е�λ��_________________ ���� Y���|(zh��)�����ʽ___________�����
��2��������C��һ���l�������ɻ�����A�Ļ��W(xu��)����ʽ_________________________������
��3�������£���Cͨ��Ԫ��Y����߃r(ji��)�������ˮ�����ˮ��Һ�����ǡ����ȫ����(y��ng)�r(sh��)��Һ��_______�ԣ���ᡱ�����A���������С�����������˕r(sh��)��Һ���x�ӝ���ɴ�С�����?y��n)�_(k��i)____________________������
��4����X��Y�����Z�������W�ķNԪ�ؽM�ɵğo(w��)�C(j��)����ʽ�}������c������NaOH��Һ�ڼӟ�l���·���(y��ng)���x�ӷ���ʽ��_(k��i)___________________������
��5����X������Z�����W���NԪ�ؿ����γɻ�����W2Z6X���������ͨ�^(gu��)�Ɵ�������~�����ɫ�������~��(hu��)��u׃�t���tԓ����(y��ng)�Ļ��W(xu��)����ʽ��_(k��i)________________________���
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ����ĩ�}
�}�ͣ��Ɣ��}
��֪A��B������C��D�������E�Ƕ����ڵ���NԪ��������������ԭ����(sh��)��������AԪ��ԭ���γɵ��x�Ӻ�����Ӕ�(sh��)����������C�����D��E���NԪ�ص���߃r(ji��)�����(du��)��(y��ng)ˮ����֮�g���ԃɃɷ���(y��ng)����A�cCͬ���������B�cEͬ�������E�Ć��|(zh��)�鵭�Sɫ���w���������ڶ���̼���
��1��Ո(q��ng)��(xi��)��A��EԪ�ص����Q��A _________����E___________�������
��2����(hu��)��CԪ�ص��x�ӽY(ji��)��(g��u)ʾ��D ___________������
��3����(xi��)��C��D����߃r(ji��)�����(du��)��(y��ng)ˮ���������(y��ng)�Ļ��W(xu��)����ʽ____________���
��4��A��B���C���NԪ���γɵĻ����������Ļ��W(xu��)�I��͞�_(k��i)_____________��
��5��B����C������D��E�ķNԪ�ص�ԭ�Ӱ돽�ɴ�С���������?y��n)�_(k��i)________ ����Ԫ�ط�̖(h��o)��ʾ�����
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ����ĩ�}
�}�ͣ����x�}
A��B�����C�����D���ķN����������Ԫ�أ���ԭ����(sh��)�������������֪A���������Ӕ�(sh��)������ӌӔ�(sh��)��2����B�ǵؚ��к� ����ߵ�Ԫ��������Bԭ�ӵ��������Ӕ�(sh��)��Dԭ���������Ӕ�(sh��)��2����Cԭ�������ֻ��һ��(g��)��������������f(shu��)�����_����
A����߃r(ji��)�����(du��)��(y��ng)ˮ����ĉA�ԣ�C < D
B����B(t��i)�仯��ķ�(w��n)���ԣ�A��B
C���ķNԪ���܉���ͬһ����
D��ԭ�Ӱ돽��C��A
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ�������}
�}�ͣ��Ɣ��}
��֪A������B����C���D��E�Ƕ�����Ԫ�����������ԭ����(sh��)��u����AԪ��ԭ���γɵ��x�ӛ](m��i)������������C����D�����E���NԪ�ص���߃r(ji��)�����(du��)��(y��ng)ˮ����֮�g���ԃɃɷ���(y��ng)�������A�cCͬ����������B�cEͬ��������E�Ć��|(zh��)���Sɫ���w�������ڶ���̼������
��1��A���x�ӷ�̖(h��o)��________���
��2��C��D����߃r(ji��)�������ˮ���������(y��ng)���x�ӷ���ʽ��________�������
��3��A����B���C���NԪ���γɵĻ����������Ļ��W(xu��)�I�����________��
��4��B������C��D���NԪ�ص��x�Ӱ돽�ɴ�С�������________���
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ�������}
�}�ͣ��Ɣ��}
W��X����Y��Z�dz�Ҋ(ji��n)�Ķ�����Ԫ����������ԭ�Ӱ돽�Sԭ����(sh��)׃�����D��ʾ�����֪W��һ�N���ص��|(zh��)����(sh��)��18��������Ӕ�(sh��)��10���X��Ne�ĺ�����Ӕ�(sh��)���1�����Y�Ć��|(zh��)��һ�N��Ҋ(ji��n)�İ댧(d��o)�w����������Z��ԭ�Ӱ돽��ͬ��������Ԫ������С����
��1��W�ĺ��ط�̖(h��o)��________�������
��2��X��Y�Ć��|(zh��)������������c(di��n)�^�ߵĻ��W(xu��)ʽ��________���
��3�������ʽ��ʾX��Z�γɻ�������^(gu��)��________��
��4��Z����߃r(ji��)�������ˮ����Ļ��W(xu��)ʽ��________������
��5��Y�cW�γɵĻ������cX����߃r(ji��)�������ˮ���ﷴ��(y��ng)���x�ӷ���ʽ��_______������
��6����25��������101kPa�£���֪Y�Ě�B(t��i)�仯������������ȫȼ���֏�(f��)��ԭ��B(t��i)������D(zhu��n)��1mol��ӷų�����190.0kJ�������ͬ��r��1molY�Ě�B(t��i)�仯����ȫȼ���ų��ğ�����________��
�鿴�𰸺ͽ���>>