
��Ŀ�� ��Դ�� �}�ͣ���x����
| ���|(zh��) | FeSO4 | H2SO4 | Ag2SO4 | Al2��SO4��2 | ���� |
| �|(zh��)���֔�(sh��)/��%�� | 15.0 | 7.0 | 0.40 | 0.34 | 5.0 |
| �ض�/�� | 0 | 10 | 20 | 30 | 40 | 50 |
| FeSO4��Һ�ȣ�g�� | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 |
| Al2��SO4��3�ܽ�ȣ�g�� | 31.2 | 33.5 | 36.4 | 40.4 | 45.7 | 52.2 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ���x����
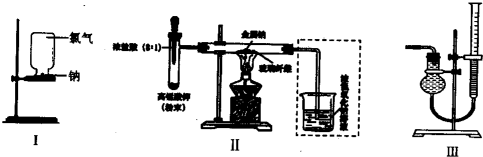
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
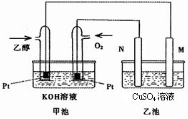
| ||
| ||
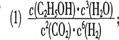
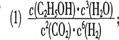
�ضȣ�K�� CO2�D(zhu��n)���ʣ�%�� n��H2��/n��CO2�� |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
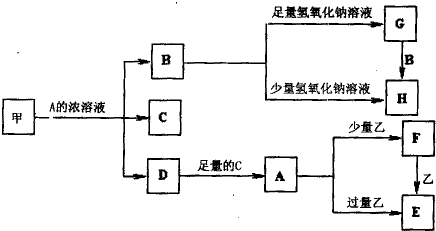
| ||
| ||
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| ���W(xu��)����(y��ng)����ʽ�����ӣ� | �����D(zhu��n)����ʽ | ||||
| �� | �ɻ��W(xu��)���D(zhu��n)������� | ||||
��Pb+PbO2+2H2SO4
|
|||||
��CaCO3
|
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
 ��D��ԭ늳��b��ʾ��D��
��D��ԭ늳��b��ʾ��D���鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| ���Ӵ�̖ | A | B | C | D | E | F | G |
| ԭ�Ӻ˂���(sh��) | �κ� | �κ� | �p�� | �ĺ� | �κ� | ��� | ��� |
| 늺ɔ�(sh��) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
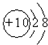
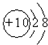
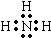
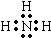
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com