
科目: 來源: 題型:
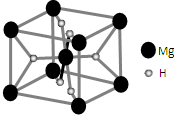 開發(fā)新型儲氫材料是氫能利用的重要研究方向.
開發(fā)新型儲氫材料是氫能利用的重要研究方向.查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:

查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
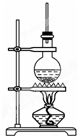 如圖為硬脂酸甘油酯在堿性條件下水解的裝置圖,進(jìn)行皂化反應(yīng)時的步驟如下:
如圖為硬脂酸甘油酯在堿性條件下水解的裝置圖,進(jìn)行皂化反應(yīng)時的步驟如下:查看答案和解析>>
科目: 來源: 題型:
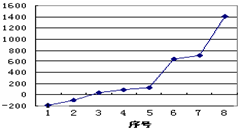 (1)第三周期8種元素按單質(zhì)熔點(diǎn)高低的順序
(1)第三周期8種元素按單質(zhì)熔點(diǎn)高低的順序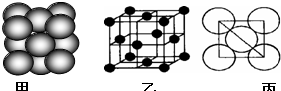
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com